
中国粉体网讯 目前,制药企业常用的制粒方式主要有干法制粒与湿法制粒两种。其中干法制粒是将原材料经过物理加工的方式制成颗粒产物,相较于湿法制粒,无需干燥,整粒等后续生产工艺,对辅料的需求量降低,载药量得到相对提升。干法制粒技术在发达国家发展较为成熟,广泛运用于食品制药领域,但我国起步较晚,在技术理论方面则较为薄弱。
制粒是制药过程关键工艺步骤之一,所得颗粒可能是最终品,用于制备胶囊和冲剂,也可能是中间体,后期根据药品用途进行包衣和压片处理,用于制备片剂。在每个环节都有重点关注的指标,在压片阶段重点关注的是片体的密度或者孔隙度,在制粒环节则为颗粒成型率,在片剂生产的环节则为拉伸强度或者药性的溶出崩解度。干法制粒作为整个固体制剂的上游工艺,制粒的效果直接影响着药效,对制粒过程中每个步骤质量的把控是制粒生产线的核心。
滚压法制粒是目前干法制粒的主要工艺方法。影响颗粒成型率与滚压结构有着密切的关系。作为一个连续的生产过程,片体的压制犹如暗箱,一般实际颗粒制备得到的是最终的成型颗粒,很难得知工艺参数对中间临界属性的影响。片体质量的好坏直接影响着制粒的质量。
干法制粒的工艺流程主要分为压片和整粒两个步骤。粉状物料通过进料斗进入输送单元,由螺杆进行送料。继而滚轮将粉末推到滚轮间隙处,粉末受到一对反向旋转的滚轮高应力的作用,从而形成致密的薄带。片体经过整粒装置的破碎作用,筛网的筛分,最终得到目标范围的颗粒。
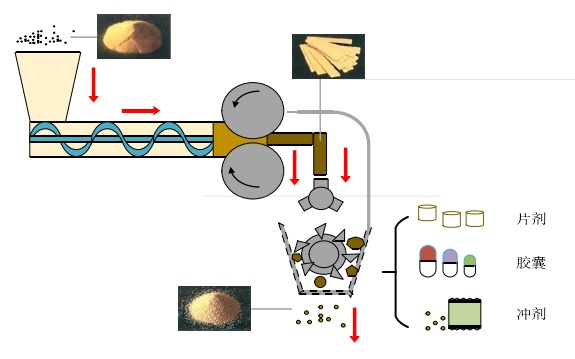
干法制粒流程
在干法制粒生产过程中,由于过多依赖经验操作,缺乏制剂原料粉体性质、工艺与质量之间定量关系的研究等问题。制剂原料的粉体性质差异、辅料用量及工艺参数的变化都有可能导致终产品成型性的波动,增加了质量控制的难度,因此制定有效应对风险的质控策略至关重要。
QbD(质量源于设计)理念在国际制药领域被广泛推行,是对药品制剂生产质量的控制方法。QbD理念于2001年由美国FDA在药品管理理念中提出,旨在将药品质量监管体系从以往单纯依赖终产品检验过渡到产品设计、生产过程和研究阶段的质量控制,阐明制剂原料性质与工艺参数对产品质量的影响规律,从而全面提升产品质量的稳定性及生产工艺的可调控性。
QbD理念在实施中需要让生产工艺参数运行在能够保证产品质量稳定的范围内,因此有必要明确生产工艺参数的设计空间。建立设计空间的主要步骤为:1.产品关键工艺参数的辨识;2.产品关键质量属性的确定;3.关键工艺单元数学模型的建立;4.设计空间的构建;5.控制空间的形成。
虽然“质量源于设计(QbD)”的产品研发理念已经被广泛认可,但由于对制剂产品的关键质量属性认知的缺失、以及产品关键质量属性与原辅料和制剂工艺相关性研究的不足,致使QbD理念的实施并不充分。因此,如何确认产品关键质量属性,并借助数学建模以及人工智能技术探索“原料-工艺-产品”之间复杂的相关性,高效、准确地设计制剂处方和工艺?是口服固体制剂开发亟需解决的瓶颈问题。
2023年9月21-22日,中国粉体网以“从粉体技术,论制药工艺”为主题,将在辽宁沈阳希尔顿逸林酒店举办“第五届全国医药粉体制备及物性表征技术高峰论坛”,本次会议特别邀请来自上海中医药大学中药现代制剂技术教育部工程研究中心的杜若飞副研究员作《数学建模技术辅助干法制粒处方与工艺设计》的专题讲解,为解决口服干法制粒处方与工艺开发过程中反复试错造成的研发效率低下问题,针对过度依赖研究人员经验引发起的制剂质量均一性、一致性、稳定性问题提供了可行的技术方法。

报告人介绍
杜若飞,博士,上海中医药大学副研究员,硕士生导师。中国中药协会中药新技术专业委员会常务理事;中国颗粒学会生物颗粒专业委员会委员;中国颗粒学会青年理事;世界中医药联合会中药制剂专业委员会委员;中华中医药学会中成药分会委员。主要研究方向为中药制剂关键技术及其基础理论研究、中药制剂开发与人工智能研究、中药新剂型研究等。近五年来,承担包括国家自然科学基金等国家级、省部级项目3项,参与项目9项。以第一(通讯)作者发表论文80余篇,授权发明专利5项。接受企业委托主持研发新药品种多项,累计项目金额600余万元。曾获2020上海市技术发明奖二等奖;2020上海中医药科技奖(著作类)三等奖;参编专著《中药固体制剂技术理论与实践》,2017年3月出版。
资料来源:
高迪.基于QbD理念的组分中药粉体性质-工艺参数-干法颗粒质量相关性研究及其预测模型的构建
高豪峥.基于物料特性的干法制粒仿真分析及质量预测研究
(中国粉体网编辑整理/青黎)
注:图片非商业用途,存在侵权告知删除
